| |
1.レチノイドの概念と作用機序
ビタミンA(レチノールretinol)とその類縁化合物であるレチノイドretinoidは、生体内では形態形成制御作用、細胞の分化増殖制御などの作用を持っている。レチノイン酸はビタミンAのカルボン酸誘導体で、all-trans
retinoic acid (tretinoinトレチノインとも呼ばれる)、9-cis retinoic acid
(alitretinoin とも呼ばれる; 9シスレチノイン酸)、13-cis retinoic acid (isotretinoinとも呼ばれる;
13シスレチノイン酸)などいくつかの立体異性体が存在する(図1)。トレチノインは核内受容体の一つであるレチノイン酸受容体(retinoic
acid receptor; RAR)の天然リガンドとして、生体内におけるレチノイド、カロテノイドの生理活性の主役を担っている。RARはレチノイドX受容体(retinoid
X receptor; RXR:リガンドは9cisレチノイン酸)とヘテロ二量体を形成し、リガンド誘導性転写因子として、特異的な標的遺伝子群のプロモーターに結合することで標的遺伝子群の発現を正負に転写レベルで制御することが知られている(図2)。RAR、およびRXRにはそれぞれα、β、γと3種類のsubtypeがあり、皮膚においてはRARα、γが発現しており、RARγが90%を占め、RXRではRXRα、βが発現しており、RXRαが大半を占めている。この他、RARが転写因子AP-1の情報伝達を妨げることにより作用することも明らかになっている1)。現在はビタミンAとは全く類似しない化学構造を持つ化合物でも、これら特異的な受容体と非常に高い結合親和性を示す合成化合物を含めて、レチノイドと称されている。
2.レチノイドの外用剤
本邦で外用剤として認可されているレチノイドはレチノール(医薬品、化粧品)および酢酸レチノールretinyl acetate、パルミチン酸レチノールretinyl
palmitateなどのレチニールエステル(化粧品)であるが、これらの薬剤では副作用はみられないが、薬理作用が小さい(トレチノインの100分の1程度)。海外を中心に現在までに認可された、もしくは開発・治験中のレチノイド製剤(内服を含む)を表1に示す。
レチノイドは脂溶性であり、オイル、ワセリンなどの基剤のままでは皮膚への浸透が極めて悪い特徴がある。また、トレチノインやオールトランスレチノールなどは光、熱による薬剤安定性が悪い。そのため薬剤の粒子自体か、基剤などに工夫する必要がある。通常レチノール油と呼ばれるものはレチニールエステルをオイルに溶かしたもので安定しているが、皮膚への浸透、成分の薬理作用ともに極めて小さい。確立されている合成レチノイドはすべて薬剤安定性は高い。
我々はトレチノインを水性ゲル基剤(0.1-0.4%)で使用しているが(表2)、親水軟膏やクリーム基剤と比較すると数倍、ワセリンとは10倍以上の皮膚浸透性の違いがある。安定性は悪いため、密封、冷蔵しても月に10%くらいのトレチノインが変性するため、毎月新しく調合している。同様の基剤でオールトランスレチノールやレチニールも濃度を数十倍に上げればトレチノインと同程度の臨床上の有効性を示したが、皮膚炎などの副作用もやはり同程度に見られることがわかった2)。
3.トレチノインの皮膚における作用およびその作用機序
トレチノインの継続的外用により、表皮においては表皮角化細胞の強い増殖促進作用がみられ表皮は肥厚し角質はコンパクトになる。レチノイドによりsuprabasal
keratinocytesからHB-EGF(heparin-binding EGF-like growth factor)が分泌されparacrineにより表皮細胞の増殖が促進される。ターンオーバーも早くなるため、結果的に表皮内のメラニンが排出される。角質の剥離が見られ、薬剤浸透性が高まるとともに、角栓が取れることによりニキビへの治療効果が見られる。
表皮角化細胞間や角質にヒアルロン酸などのムコ多糖類の沈着を促し3)、短期的には表皮のresurfacing効果がある。メラノサイトに対するメラニン産生の抑制効果には否定的な見解が多い4)。さらに、真皮においては線維芽細胞のコラーゲン産生促進、MMP抑制などの作用で光老化に対する抑制効果がある。その作用機序には、紫外線により発現亢進するc-Junによって引き起こされるprocollagen転写の抑制をトレチノインが妨げる5)、抗AP-1作用によりMMPの発現を抑制する(光老化によってMMP-1、MMP-8の発現が亢進する)、また紫外線によるTGF-βシグナルの抑制を防ぐ、などが指摘されている6)。したがって長期使用によって老化による真皮の菲薄化を抑え、皮膚の張りを取り戻すことが期待される。皮脂の分泌を抑制する働きも持つ。また、真皮乳頭層の血管新生が見られ、表皮、真皮レベル双方で皮膚の創傷治癒を促進する働きを持っている。
4.トレチノインによるしみ治療の原理
トレチノインは表皮内のメラニンの排出を促す作用があり、それは①表皮角化細胞を増殖させること、および②表皮ターンオーバーを早めること、によると思われる。メラノサイトに対してのチロジーナーゼ活性抑制、細胞毒性、メラニン産生抑制などの直接的効果は実験的には認められない4)。
トレチノインによる表皮の肥厚はin vivoにおいて普遍的に見られるがその作用機序は長い間不明であった1)。表皮角化細胞の単層培養ではレチノイドの影響はばらつきが多く、一方、皮膚の器官培養や表皮角化細胞と線維芽細胞のみの3次元培養では安定した効果が確認されたが、その仲介物質、メカニズムに関しては不明であった。1999年トランスジェニックマウスを使った研究報告7)がきっかけとなり、レチノイドはsuprabasal
keratinocyteからHB-EGFmRNAおよび蛋白の発現を誘導することがわかった(basal keratinocyteからは非常に少ない)。HB-EGFmRNAのプロモーター部位にはレチノイド受容体の認識配列はないため、さらに仲介するメカニズムが存在する可能性もある。実際、ヒト表皮角化細胞でも分化誘導をかけるとレチノイドによりHB-EGFmRNAの発現が亢進し、このHB-EGFmRNA誘導作用は受容体選択性の異なるレチノイドの種類により大きく異なっていたが8)、レチノイド受容体へテロ二量体群の中でもRARγ-RXRαが仲介していることが明らかにされた9)。レチノールやレチナールによっても高濃度であれば実験的にHB-EGFmRNAが誘導されること8)、また臨床的にもメラニン排出効果があること、が明らかとなったが、皮膚炎などの副作用も同程度に現れることがわかり2)、現在までのところ効果を維持したまま副作用を減らす有効な解決策はない。
トレチノインの外用により組織学的には2週間程度の短期間で、表皮の肥厚、劇的な表皮メラニンの減少が認められる(図3)。しかし、2ヶ月程度の長期間の治療でも真皮メラニンの減少は見られない10)。
4.レチノイドによる耐性の獲得
皮膚にレチノイドの外用を続けると当初見られた落屑、紅斑を伴う皮膚炎は段々なくなっていく。レチノイド外用剤の濃度をいくら上げても同じことが起こる。これをレチノイドの耐性の獲得という。これはレチノイドの内服治療においても同様のことが見られる。副作用がなくなって使いやすくなったようにみえるが、実際にはレチノイド特有のシグナル伝達自体が抑えられている。耐性獲得の原理は明らかとされていないが、1つの理由にレチノイドによって直接upregulateされるCRABPII(cellular
retinoic acid binding protein II)が細胞質内で遊離のトレチノインを捕捉し核内への移行を妨げていることがレチノイドシグナルに共通するnegative
feedback機構として働いている可能性が挙げられる。
5.副作用
レチノイド外用剤の副作用は、皮膚炎症状(落屑、紅斑、irritationなど;皮膚内RARの90%を占めるRARγを介した作用であると考えられている)、それによる炎症後色素沈着の可能性であり、さらに催奇性も問題となりうる。炎症後色素沈着は強い刺激がなければハイドロキノンの併用で防ぐことが可能であるが、皮膚炎については、薬理作用を減じずに回避する手段はないのが現状である。
外用における催奇形性については実際に吸収され血中に入る量を投与量、吸収率などから考慮すると内服薬の千分の一のオーダーであり、非常に低いと考えられる(この場合それぞれのレチノイドの半減期の長さも問題になる)。米国ではレチノイン酸"外用"では催奇形性はありえないと結論付けられ、仮に注意するとしても"妊娠している女性"のみで十分であるとする意見が多い。著者は若い患者には使用中は避妊を励行するように指導している。
6.治療法と治療適応
メラニンの少ない白人では紫外線による光老化治療のメインターゲットは小じわ、毛細血管拡張などの真皮性の変化、および皮膚の癌化である。メラニンの多い東洋人の場合には美容的には老人性色素斑などの色素沈着の愁訴が最も多く、白人の場合とは異なっている。したがって、欧米ではトレチノイン外用剤は海外で若返り目的で使用する場合には、広範囲にマイルドな投与が行われ、ハイドロキノン(HQ)を色素沈着治療を目的に併用する場合には、色素沈着の部分にのみHQが使用されることが多い。ところが色素沈着を目的とする場合には、トレチノインの表皮メラニン排出作用を引き出すために投与量を多くする必要がある。我々は、副作用である皮膚炎を誘発するため色素沈着の部分にのみ強い治療を行い、HQは治療に伴いうる炎症後色素沈着を予防するために顔全体など広範囲に使用する治療法を提唱し、以前には認められなかった大きな漂白効果を実現している11-13)。基本的治療プロトコールを図4に示す。前半は漂白期間(bleaching
phase)で、後半は皮膚炎症状を炎症後色素沈着を引き起こさないように冷ましていく治癒期間(healing phase)である。
以上のように、①小じわ、にきびなど対象としたマイルドな投与、②表皮メラニンの排出(しみの治療)を目的としたアグレッシブな治療、があり、前者は副作用が小さいため広範囲な治療が可能であり、後者は、皮膚炎を誘発するので、および色素沈着の部分のみを漂白するために、局所的な治療が行われる。
トレチノインによる漂白治療の治療適応は、一言で言えば"角質肥厚のない表皮内メラニン沈着"である。特にレーザー適応のない①肝斑、②炎症後色素沈着、に対しては有効性も高く、第一選択と言える。日光性色素斑(老人性色素斑)の場合には角質の肥厚がある場合があり、その場合にはQスイッチレーザーを優先し、その後の炎症後色素沈着にトレチノインを使用する。雀卵斑、扁平母斑は再発しやすいが、顔面であれば有効性は高い。漂白治療後はHQ単独の使用で良好な状態を維持できる。
ADM(後天性真皮メラノサイトーシス)や種々の黒皮症など、表皮と真皮双方にメラニンが存在する疾患の場合には、始めにトレチノイン治療を行って表皮メラニンのみを排出することにより、その後のレーザー治療の効率が上がるとともに、レーザー治療による炎症後色素沈着が起こり難くなる(表皮内メラニンの減少のため)10)。
炎症後色素沈着の効果的治療法を持つことの臨床的意義は大きく、東洋人に対してこれまで炎症後色素沈着のためにはばかれていた、よりアグレッシブなレーザー治療やresurfacing治療が容易に行えるようになった。
参考文献
1) Fisher GJ, Voorhees JJ: Molecular mechanism of retinoid
actions in skin. FASEB J. 10:1002-1013, 1996.
2) Yoshimura K, Momosawa A, Aiba E, Sato K, Matsumoto D,
Mitoma Y, Harii K, Aoyama T, Iga T. Clinical trial of bleaching
treatment with 10% all-trans retinol gel. Dermatologic Surgery
29: 155-160, 2003.
3) Kligman AM, Grove GL, Hirose R, Leyden JJ: Topical tretinoin
for photoaged skin. J. Am. Acad. Dermatol. 15:836-59,1986.
4) Yoshimura K, Tsukamoto K, Okazaki M, Virador VM, Lei
TC, Suzuki Y, Uchida G, Kitano Y, Harii K. Effects of all-trans
retinoic acid on melanogenesis in pigmented skin equivalents
and monolayer culture of melanocytes Journal of Dermatological
Research, 27(S1): 68-75, 2001.
5) Fisher GJ, Datta S, Wang Z, Li XY, Quan T, Chung JH,
Kang S, Voorhees JJ. c-Jun-dependent inhibition of cutaneous
procollagen transcription following ultraviolet irradiation
is reversed by all-trans retinoic acid. J Clin Invest. 2000
Sep;106(5):663-70.
6) Kang S, Voorhees JJ: Photoaging therapy with topical
tretinoin: an evidence-based analysis. J. Am. Acad. Dermatol.
39: S55-61, 1998.
7) Xiao J H, Feng X, Di W, et al. Identification of heparin-binding
EGF-like growth factor as a target in intercellular regulation
of epidermal basal cell growth by suprabasal retinoic acid
receptors. EMBO J 1999: 18:1539-1548.
8) Yoshimura K. Uchida G. Okazaki M. Kitano Y. Harii K.
Differential expression of heparin-binding EGF-like growth
factor (HB-EGF) mRNA in normal human keratinocytes induced
by a variety of natural and synthetic retinoids. Experimental
Dermatology, 12(Suppl.2): 28-34, 2003.
9) Chapellier B, Mark M, Messaddeq N, Calleja C, Warot X,
Brocard J, Gerard C, Li M, Metzger D, Ghyselinck NB, Chambon
P. Physiological and retinoid-induced proliferations of
epidermis basal keratinocytes are differently controlled.
EMBO J. 2002 Jul 1;21(13):3402-13.
10) Momosawa A, Yoshimura K, Uchida G, Sato K, Aiba E, Matsumoto
D, Mihara S, Tsukamoto K, Harii K, Aoyama T, Iga T. Combined
Therapy Using Q-Switched Ruby Laser and Bleaching Treatment
with Tretinoin and Hydroquinone for Acquired Dermal Melanocytosis.
Dermatological Surgery, 29: 1001-1007, 2003.
11) Yoshimura K, Harii K, Shibuya F, Aoyama T, Iga T: A
new bleaching protocol for hyperpigmented skin lesions with
a high concentration of all-trans retinoic acid aqueous
gel. Aesthetic Plast. Surg. 23: 285-291, 1999.
12) Yoshimura K, Harii K, Aoyama T, Iga T. Experience of
a Strong Bleaching Treatment for Skin Hyperpigmentation
in Orientals. Plastic and Reconstructive Surgery, 105: 1097-1110,
2000.
13) Yoshimura K, Momosawa A, Watanabe A, Sato K, Matsumoto
D, Aiba E, Harii K, Yamamoto T, Aoyama T, Iga T. Cosmetic
color improvement of the nipple-areola complex by optimal
use of tretinoin and hydroquinone. Dermatologic Surgery
28:1153-1157, 2002.
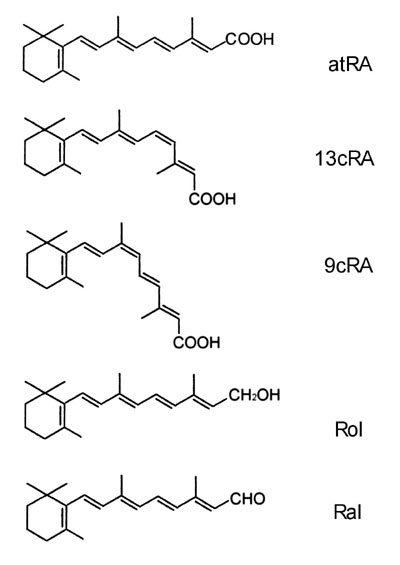
図1.代表的天然レチノイドの構造式。atRA:オールトランスレチノイン酸、13cRA:13シスレチノイン酸、9cRA:9シスレチノイン酸、Rol:オールトランスレチノール(ビタミンA)、Ral:オールトランスレチナール
|
|

